当研究室では、下記のようなテーマの研究を進めています。
3. これらの制御が破綻した状態としての白血病をはじめとしたさまざまな疾患の病態解明
造血幹細胞や単球がどのようにして生命を支えるという基本的な仕組みを解明し、その知見に基づいた疾患の病態解明と、治療や予防法の確立を目指しています。国内外の多くの研究室との共同研究にも積極的に取組んでいます。
1. 造血幹細胞の制御機構解明
組織幹細胞
人体は数十兆もの細胞から構成されていますが、個々の細胞の寿命には限りがあります。そのため、多数の細胞から構成される体が長年にわたって維持されるためには、必要な細胞が絶えず供給される必要があります。このような需要に応じた細胞を供給し続ける仕組みの一つが幹細胞システムです。体内のさまざまな組織に存在する“組織幹細胞”は、さまざまな種類の細胞へ分化する能力のみならず、自らを複製する能力を兼ね備えており、生涯にわたる臨機応変かつ適切な細胞供給によって生命を支えています。
造血幹細胞
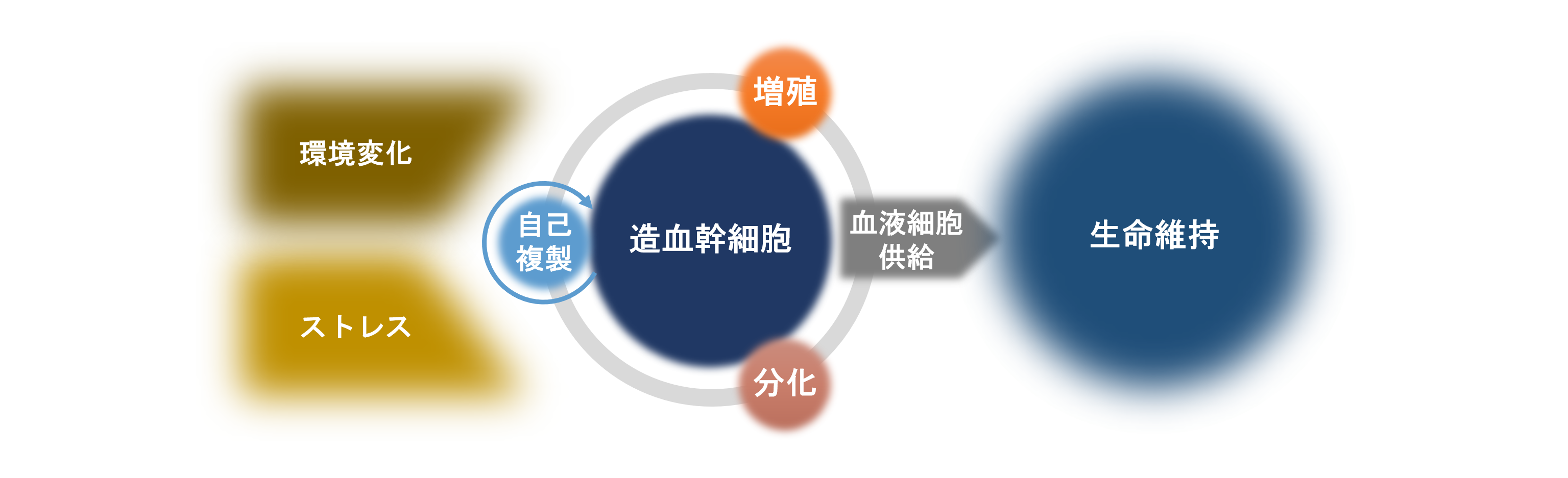
骨髄の中に存在する造血幹細胞は、組織幹細胞の一つで、血液の中に存在する赤血球、血小板、白血球のすべてを産み出す能力を備えています。血液細胞の数は、通常は一定レベルに維持されていますが、環境の変化やストレスに応じて大きく変動するため、その供給原となる造血幹細胞は、体内でもっともダイナミックに変化する幹細胞といえます。したがって、その制御機構は生命維持・健康維持の基本的なメカニズムとして極めて重要ですが、まだ十分に理解が進んでいません。
ストレス造血の制御
感染を始めとした炎症や抗がん剤などのストレスが加わると、造血幹細胞は好中球や単球など骨髄球系と言われる細胞を多数供給するように制御されます。私たちの研究室では、このようなストレス負荷時の造血制御の"要"となる遺伝子としてロイシンジッパー型の転写因子C/EBPβを同定しています。このC/EBPβを軸として、① C/EBPβの発現がどのように制御されているのか、② ストレス負荷時にC/EBPβは造血幹細胞の運命決定をどのように制御しているのか、③ ストレス解消時の定常状態への復帰機構などストレス負荷時の造血制御機構の包括的な解明を目指しています。
Vanickova K et al. EMBO J. 42(23), e113527, 2023
Sato A et al. Blood Adv. 4(14):3343-56, 2020
Satake S et al. J Immunol. 189(9): 4546-55, 2012.
2. 単球の分化制御機構と新規単球の機能の解明
単球
単球は全ての白血球のプロトタイプともいうべき細胞で、進化的には造血幹細胞よりも先に生じたと考えられています。単球は、病原微生物を貪食したり、その情報を他の免疫担当細胞に伝えたりする役割を持つことが知られています。単球や単球に由来するマクロファージは、動脈硬化や癌など、感染症・炎症性疾患に限らず多彩な疾患への関与が判明しており、その産生調節や、機能の正確な理解は非常に重要な課題です。
新規単球亜分画の発見
従来、単球は均一な細胞集団と考えられてきましたが、最近になって複数の異なる細胞亜集団から構成されることがわかってきました。当研究室では、新たな単球の亜集団(CD135+単球)を世界に先駆けて発見しました。この単球は、従来から知られている他の単球亜集団や、同様にCD135を発現する樹状細胞とはまったく異次元の機能を備えている可能性を示唆するデータが蓄積しています。また、造血幹細胞から新規単球が作り出される過程を検討する中で、新たな単球の分化経路・分化制御機構を見出しつつあります。この研究が、新しい分野を切り開く発見につながる可能性が高いと考えて、日々実験を積み重ねています。
Kamio N & Yokota A et al. J Immunol. 209(3):498-509, 2022
Tamura A et al. Blood. 130(16):1809-18, 2017
3. 白血病をはじめとした疾患の病態解明
白血病
白血病は、遺伝子変異によって造血幹細胞や前駆細胞が異常増殖するために生じる疾患です。従来は、定常状態における造血制御機構の破綻がその発症機構として注目されてきました。ところが、最近になって私たちが見出したC/EBPβによる造血幹細胞や前駆細胞の制御のようなストレス造血制御機構が、いわば"ハイジャック"のような形で白血病細胞に"悪用"されているということがわかってきました。当研究室では、どのようにしてC/EBPβが白血病の病態に関わっているのかについて、正確な分子メカニズムを明らかにすることによって、新たな治療標的分子の探索など治療法の開発を目指しています。
炎症・自然免疫記憶・クローン性造血
血液細胞の数の変動は、感染症や炎症性疾患のみならず、多くの疾患において認められ、その測定は、あらゆる疾患の診断において欠かせない検査となっています。その意味で造血幹細胞はすべての疾患との関連があるといっても過言ではありません。一方、造血幹細胞は、環境変化や、炎症などのストレスに応じて受動的に反応するのみと考えられてきましたが、最近になって環境変化やストレスを造血幹細胞が記憶していること(自然免疫記憶)、老化に伴って遺伝子変異を獲得した造血幹細胞が増加し(クローン性造血)、それに由来する血液細胞が炎症を惹起して動脈硬化性疾患、がん、代謝異常などのリスクとなることが明らかとなってきました。
したがって、造血制御機構を明らかにすることは、幹細胞システムによる生命の維持という基本原理を明らかにするにとどまらず、幅広い疾患の病態解明・治療法・予防法開発に欠かせない重要な研究テーマとなっており、私たちはこの観点からも研究に取り組んでいます。
Yokota A et al. Blood Adv. 3(3):476-88, 2019
Yokota A et al. Leukemia. 31(12):2742-2751, 2017